DynaMesh®-VASA

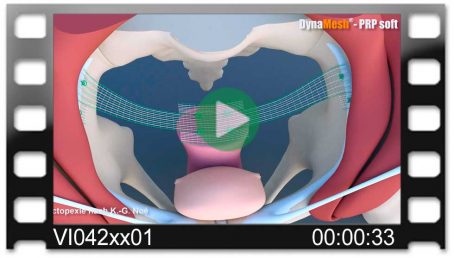
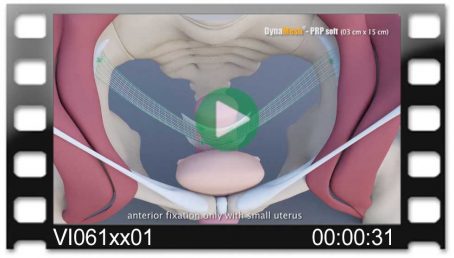
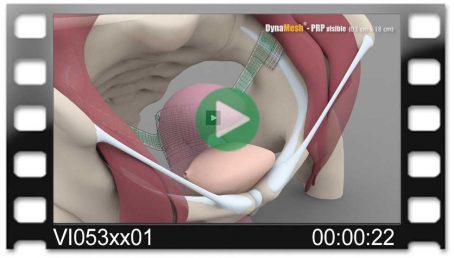
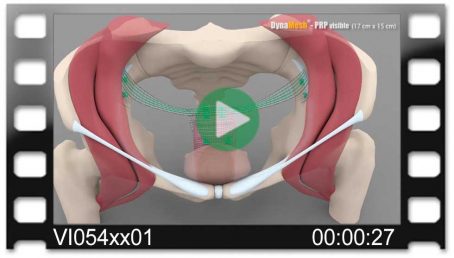
DynaMesh®-VASA Implantate wurden speziell für die Beckenbodenrekonstruktion, insbesondere zur Verstärkung oder zum Ersatz der Utero-Sakralen-Ligamente, in laparoskopischer oder offener Operationstechnik entwickelt.
Die Implantate kommen zur Anwendung bei der Behandlung eines Deszensus des inneren Genitales, wie dem Vaginalstumpfvorfall.
DynaMesh®-VASALieferprogrammAnwendung und EigenschaftenVideosDownloadsLiteratur

DynaMesh®-VASA
(VAgino-SAkropexie)
Die Operationsmethode VASA stellt ein modifiziertes Verfahren der abdominalen Kolposakropexie dar (laparoskopisch/offen), bei dem die Utero-Sakralen-Ligamente beidseitig durch das Implantat verstärkt bzw. ersetzt werden.

DynaMesh®-IVT02 Instrument zur retroperitonealen Bandanlage von DynaMesh®-VASA bei laparotomischem Zugang. Wiederverwendbares Instrument aus chirurgischem Stahl.
Länge: 32 cm.

- Extraperitoneales Tunneln
- Anatomisch dem Becken angepasst
- Öse an der Instrumentenspitze mit abgeschrägten, atraumatischen Kanten
- Einsatz bei der Laparoskopie
- Wiederverwendbares Instrument

| DynaMesh®-VASA |
02 cm x 03 cm | PV740203F1 | VE = 1 Stück |
| DynaMesh®-VASA |
02 cm x 03 cm | PV740203F3 | VE = 3 Stück |
| Produkt | DynaMesh®-VASA |
| Einsatzgebiet | Vaginalstumpfvorfall |
| Chirurgischer Zugang | laparoskopisch / offen |
| OP-Technik | Kolposakropexie (VASA) bilateral |
| Fixation an Vaginalstumpf |
Naht
|
| Fixation am Sakrum |
Naht / Tacker
|
| Speziell gewirkte, glatte Kante |
|
| Formstabilität |
|
| Definierte Elastizität |
|
| Visible Technologie |
|
| Polymer (Monofilament) |
PVDF
|
| Biokompatibilität | |
| Alterungsbeständigkeit | |
| Dynamometrie | |
| Weiterreißfestigkeit | |
| Klassifikation (Klassifikation nach Klinge [8]) | 1a |
![]() trifft für alle Produktgrößen zu
trifft für alle Produktgrößen zu